近年、腸内細菌叢や腸内フローラ、腸内環境といった言葉を目にするようになりましたが、これらは何を意味しているのでしょうか?
腸内には1,000種を超える細菌などの微生物が生息しており、これらをまとめて腸内細菌叢または、腸内フローラと呼びます。私たちの小腸や大腸などの消化管は、さまざまな物質を分泌することでこの腸内細菌叢を制御しています。この腸内細菌叢やその代謝産物、腸粘膜からの分泌物、さらには毎日摂取している食物成分が腸管内には存在しており、これらをまとめて腸内環境と呼んでいます。
腸内環境の悪化がもたらす健康への影響
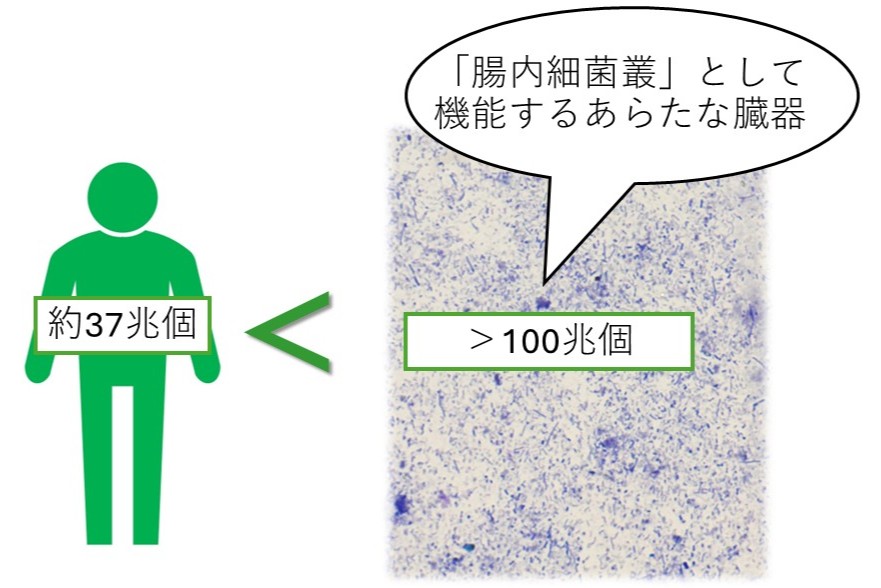
肝臓や心臓といった臓器は、細胞の集団で構成されており、人間の体はおよそ37兆個の細胞で構成されていることが明らかになっています。
細菌は1個の細胞で構成される生物ですが、人間の腸内には100兆個を超える細菌が生息していることが分かっています。すなわち、腸内細菌叢はさまざまな代謝活動を行う細菌の集合体と考えることができるため、「もう一つの臓器」として注目されるようになってきています(図1)。
心臓が悪ければうっ血や浮腫(むくみ)、場合によっては肺水腫のような呼吸器障害や腹水にもつながりますし、血液循環が悪化することで膵炎や血栓症のような他の臓器の合併症も発生します。
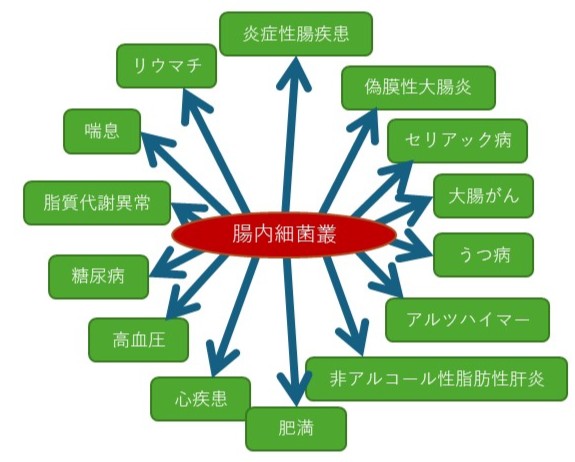
同じように、臓器としての腸内細菌叢が悪化すると、腸炎のような消化器疾患だけではなく、アトピー性皮膚炎や糖尿病、うつ病などのさまざまな疾患の原因になり得ることが分かってきています(図2)。これは、腸内細菌叢が産生する代謝産物の変化が影響していると考えられています。
さらに、腸内細菌叢は身体の免疫システムを調整する機能があることも明らかとなっています。2025年のノーベル賞で話題となった制御性T細胞は、炎症を抑える役割を持つリンパ球ですが、この制御性T細胞を増やすには腸内細菌叢が重要となります。
腸内環境の悪化はさまざまな疾患の原因にもなりますが、腸内環境を改善させれば、さまざまな炎症性疾患や免疫疾患が予防できる可能性があるといえます。そのため、腸内環境の改善が推奨されるようになってきています。
犬と猫の腸内環境の特徴
犬と猫の腸内環境に関する情報はまだ限られていますが、意外にも人間と比べて大きな違いはないことが分かってきています。細かい菌種の相違はありますが、腸内細菌叢全体が保有する消化酵素や、産生される代謝産物などはかなり類似していることが知られています。つまり、人間とは食性の異なる犬ならでは・猫ならではの菌種はあれど、「腸内細菌叢という臓器」全体で考えると、その機能に大きな差異はないと考えられています。

犬や猫における、腸内環境が原因とされる疾患
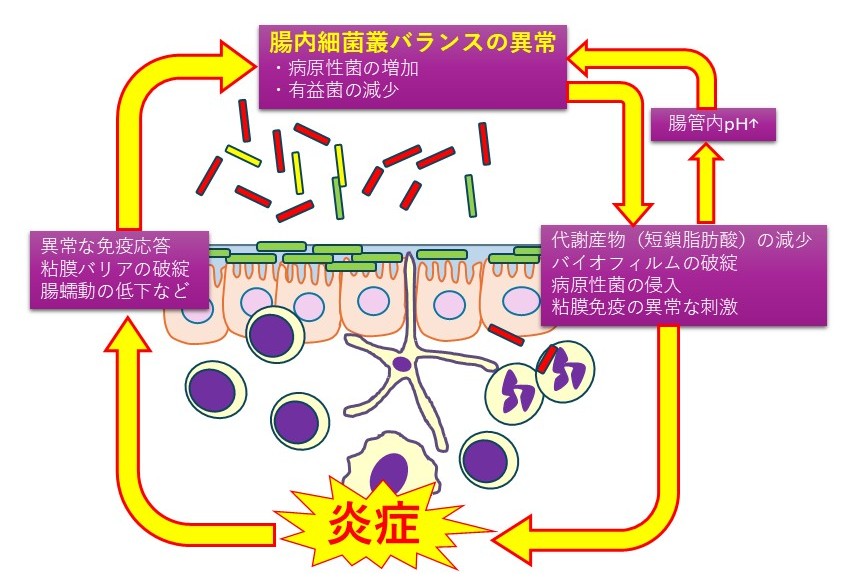
腸内環境が原因で発生する疾患としてイメージしやすいのは、慢性腸炎のような消化器疾患ではないでしょうか。腸内環境が悪化することで、腸粘膜に異常な炎症が発生して腸内細菌叢の制御ができなくなり、腸内環境がさらに悪化するという悪循環に陥っていきます(図3)。そのため、消化器疾患の治療では、腸内環境の改善が重要なものの一つと考えられるようになってきています。
犬の場合、腸内細菌叢の栄養素代謝機能の異常に伴う肥満症に加えて、肝・腎機能障害や免疫バランスを崩すことで発症するアトピー性皮膚炎、関節炎のような炎症性疾患・自己免疫性疾患の発生に関連することが報告されています。
猫においても、腸内環境の異常が肥満症や糖尿病、肝機能障害などの代謝性疾患に関連することが明らかになってきており、近年では猫に多く発生する慢性腎臓病にも関連することが指摘されています。

おわりに
犬や猫の腸内環境に関する研究は人間と比べるとまだ少ないですが、腸内環境が悪化することで発生する疾患や腸内環境を改善させるための予防・治療法に大きな違いはありません。
後編(2026年3月公開予定)では、こうした腸内環境を改善させるために、犬や猫に対してできることを解説していきます。
[参考文献]
・Qin J, Li R, Raes J, et al. “A human gut microbial gene catalogue established by metagenomic sequencing”. Nature, 464:59-65, 2010.
・Wernimont SM, Radosevich J, Jackson MI, et al. “The Effects of Nutrition on the Gastrointestinal Microbiome of Cats and Dogs: Impact on Health and Disease”. Frontiers in Microbiology, 11, 2020.
・Possemiers S, Bolca S, Verstraete W, et al. “The intestinal microbiome: a separate organ inside the body with the metabolic potential to influence the bioactivity of botanicals” Fitoterapia, 82, 2011.
・Nagpal R, Yadav H, Marotta F. “Gut microbiota: the next-gen frontier in preventive and therapeutic medicine?” Front Med (Lausanne), 1, 2014.
・Barko PC, McMichael MA, Swanson KS, et al. “The Gastrointestinal Microbiome: A Review”. J Vet Intern Med, 32, 2018.
・Honneffer JB, Minamoto Y, Suchodolski JS. “Microbiota alterations in acute and chronic gastrointestinal inflammation of cats and dogs”. World J Gastroenterol, 20, 2014.
・Yang B, Zhong S, Wang J, et al. “Dietary Modulation of the Gut Microbiota in Dogs and Cats and Its Role in Disease Management”. Microorganisms, 13, 2025.
・Deng P, Swanson KS. “Gut microbiota of humans, dogs and cats: current knowledge and future opportunities and challenges”. Br J Nutr, 113.
・Dupouy-Manescau N, Meric T, Senecat O, et al. Updating the Classification of Chronic Inflammatory Enteropathies in Dogs. Animals (Basel), 14, 2024.
・ Summers S, Quimby J. “Insights into the gut-kidney axis and implications for chronic kidney disease management in cats and dogs. Veterinary journal, 306, 2024;
【執筆者】
五十嵐寛高(いがらし・ひろたか)
獣医師。麻布大学獣医学部獣医学科 小動物内科学研究室 准教授。2005年に北海道大学を卒業し、動物病院勤務や東京大学での研修医・大学院、酪農学園大学勤務を経て現在。犬や猫を中心に、腸内細菌叢制御による疾患予防法の研究・開発を行っている。共著に『新 伴侶動物治療指針3』、『犬の内科診療 Part 3』、『猫の診療指針 Part 2』(いずれも緑書房)など。
「いきもののわ」では、ペットや動物園・水族館、野生動物、動物関連イベントなど、いきものにまつわる様々な情報をお届け中!
メールマガジンでは、特集記事の紹介や次月特集の一部をチョイ見せ!
登録はこちらのフォームから。ぜひご登録ください!
各種SNSも随時更新中! ぜひフォローしてください!